近日,我校第二臨床醫學院(東方醫院)胡凱文教授、周天副教授和中科院理化技術研究所饒偉教授團隊聯合在 Materials Horizons 上以“Autologous Cancer Cryoablation Mediated Nanovaccine Augments Systematic Immunotherapy”為題,在線發表了關于黃芪多糖納米腫瘤疫苗聯合冷凍消融治療癌癥的研究論文(IF="15.717,JCR" 1區,中科院1區),展示了黃芪多糖納米腫瘤原位疫苗用于癌癥治療的突破性成果。團隊創新性地合成中藥納米腫瘤原位疫苗,利用微創冷消融手術后腫瘤碎片作為自體抗原,靶向淋巴結,激活機體腫瘤抗原特異性免疫,從而以局部治療引發系統性抗癌免疫效應,為晚期癌癥患者帶來新的希望。這也是對中醫理論“衛行脈外”在癌癥治療領域的新詮釋。該研究得到了國家自然科學基金項目和國家重點研發計劃項目的資助。

晚期癌癥患者常因遠端轉移問題,失去根治機會。近年,隨著局部消融手術在腫瘤臨床的廣泛應用,極少部分患者在局部消融手術后出現遠端腫瘤(非消融灶)的縮小,這就是所謂的“遠端效應”。這可以認為是一種免疫效應,但總體上其發生率極低。如何大幅提升遠端效應發生的概率,從而增加癌癥患者生存期?這是一個迫切的臨床需求。如何解決這一問題?自體腫瘤原位疫苗可能是一種新思路。它能準確地將病人自身的腫瘤特異性抗原和免疫佐劑傳遞給抗原提呈細胞(主要是樹突狀細胞,DCs),從而誘導抗原特異性免疫反應,引發遠端效應,達到“牽一發而動全身”的治療目的。
《黃帝內經》中即有“營在脈中,衛在脈外,營周不休”的理論。歷代中醫學家認為,衛氣司衛外功能,屬于陽氣的一種,生于水谷,行于脈外,具有溫養、護衛、防御等重要功能。在中醫腫瘤臨床方面,扶正為主、提升衛氣功能為各派醫家認同。如何更加精準地實現扶正、提升護衛功能,一直為臨床研究者探索。
該聯合團隊長期從事冷凍消融治療腫瘤的臨床及基礎研究,曾共同開展了國際首臺冷熱復合治療系統的臨床實驗。在此最新研究中,該團隊總結了數十年冷凍消融臨床研究,為促進和強化冷凍消融的“遠端效應”, 同時結合中藥免疫佐劑特點,以中醫腫瘤臨床最為常用的補氣藥黃芪為切入點,設計了高效抓取冷凍消融碎片的納米腫瘤疫苗,提出了黃芪多糖納米腫瘤疫苗與冷凍消融手術聯合應用的癌癥治療模式,該方法除對局部腫瘤進行有效殺傷外,同時具有激活全身的腫瘤抗原特異性免疫、抑制遠端及轉移瘤體生長的重要作用。
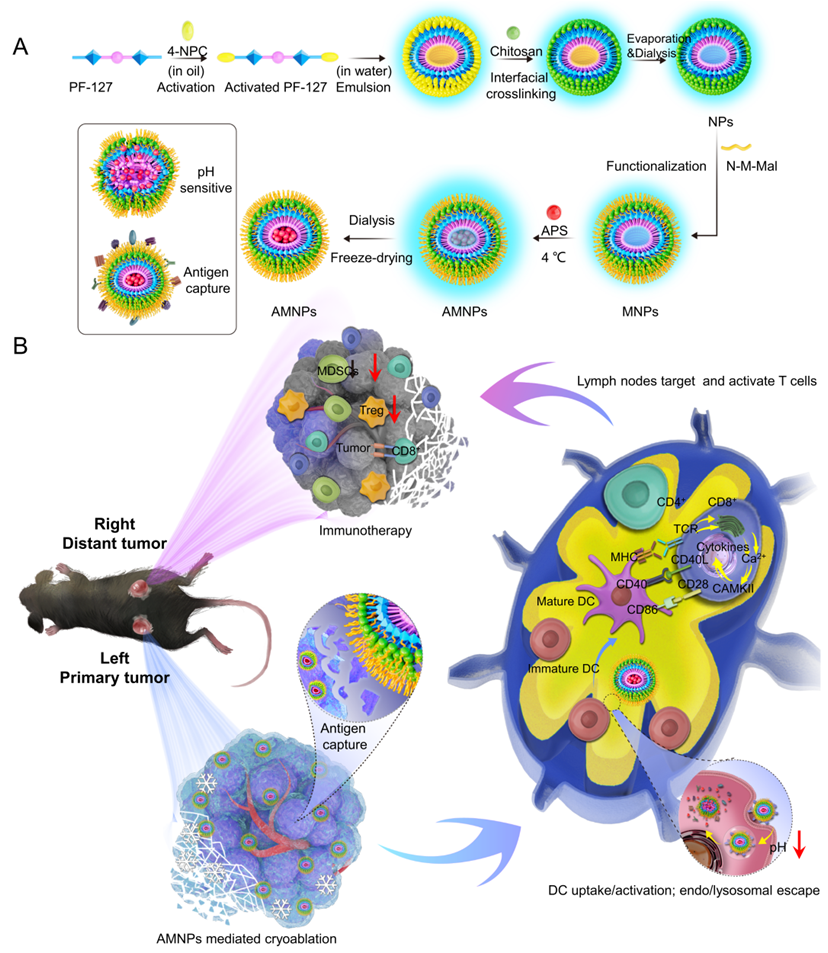
工作思路示意圖
該團隊設計的黃芪多糖納米腫瘤疫苗,通過表面修飾后,可吸附冷凍消融后的腫瘤碎片(抗原),靶向呈遞至淋巴結中,在樹突狀細胞內部通過PH響應釋放腫瘤抗原及黃芪多糖以激活抗原特異性的全身免疫治療。研究者通過對粒徑的控制,可有效地阻止納米顆粒被血液代謝,更多AMNPs進入淋巴管回流進而進入瘤周淋巴結。該納米材料具有卓越的腫瘤抗原吸附能力,可被DC細胞吞噬,并具有溶酶體逃逸功能,可有效地促進DC細胞成熟,并具有很好的生物安全性。研究者通過小動物活體成像技術,充分證實了AMNPs在活體內的代謝及淋巴結靶向功能,以及冷凍消融可以延緩AMNPs在腫瘤區域的代謝,可望增加腫瘤抗原的吸附。
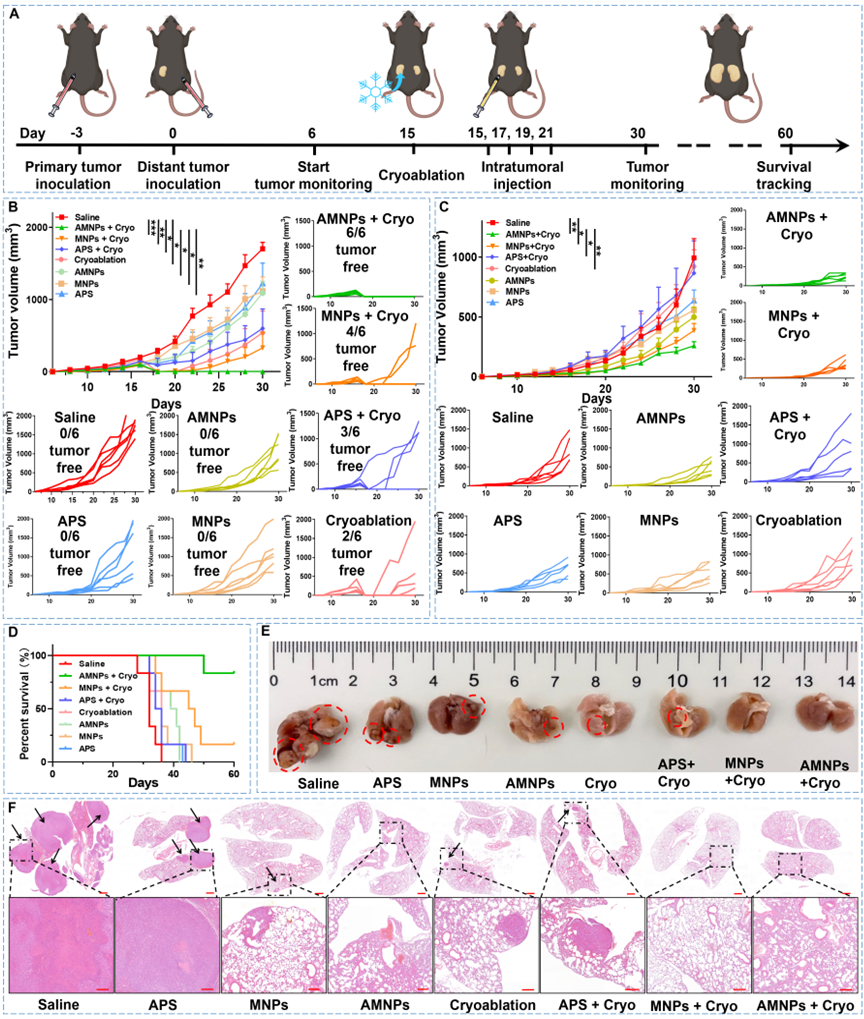
活體實驗
在雙側Lewis肺癌腫瘤模型中,AMNPs介導的冷凍消融可以明顯地使原發腫瘤消退,腫瘤生長抑制率為100%,復發率為0%(30天)和16.67%(60天),抑制未經治療的遠端腫瘤生長(與生理鹽水組相比減少約3.84倍),并最終提高長期生存率(83.33 %)。研究者還利用流式細胞術,充分證實了該聯合療法可增加消融病灶與遠端病灶中CD8+T及MHC-II+DC細胞的浸潤,降低腫瘤微環境中免疫抑制細胞的數量(MDSCs,Tregs),并通過轉錄組學檢測初步探討了聯合治療的潛在作用機制。最后,研究者利用OVA特異性四聚體,在LLC-OVA雙瘤小鼠模型中檢驗了腫瘤抗原特異性免疫的激活情況,結果提示在脾臟和淋巴組織中,腫瘤抗原特異性CD8+T細胞及MHC-I+DC的數量均顯著增加。
綜上,該團隊受中醫理論啟發,開發了一種可靶向淋巴結的黃芪多糖納米腫瘤原位疫苗,在與冷凍消融聯合應用的情況下,可實現腫瘤抗原特異性免疫激活,有效抑制了遠端及轉移瘤體生長,重塑了遠端腫瘤區域的免疫微環境。該工作首次提出了腫瘤疫苗與冷凍消融聯合的應用策略,創新性制備了與冷凍消融適配的黃芪多糖納米腫瘤疫苗,具有重大臨床應用前景。
北京中醫藥大學研究生院于中陽博士和中科院理化所汪達偉博士為本論文共同第一作者,北京中醫藥大學東方醫院周天副教授、中科院理化技術研究所饒偉教授和北京中醫藥大學東方醫院胡凱文教授為本論文共同通訊作者。
原文鏈接:
DOI:10.1039/d3mh00092c
